Les maladies cardio-vasculaires (MCV) représentent la principale cause de mortalité en France comme dans les pays industrialisés. Elles sont essentiellement dues à l’athérosclérose, une pathologie évolutive qui conduit à la formation de plaques qui obstruent les artères. L’athérosclérose est multifactorielle, mais il est bien établi qu’elle est principalement induite par un excès de cholestérol, en particulier le LDL- cholestérol (aussi appelé « mauvais cholestérol).
La quasi-totalité des méthodes et matériaux de référence permettant d’assurer la traçabilité métrologique et la fiabilité des examens relatifs aux anomalies lipidiques portent sur la mesure du cholestérol total et très peu concernent le LDL-cholestérol (une sous-classe de lipoprotéines).
Objectif
Développer de nouvelles méthodes de référence et des matériaux de référence certifiés pour l’énumération des différentes sous-classes de lipoprotéines
Résumé et résultats
Les maladies cardio-vasculaires (MCV) représentent la principale cause de mortalité en France comme dans les pays industrialisés. Elles sont essentiellement dues à l’athérosclérose, une pathologie évolutive qui conduit à la formation de plaques qui obstruent les artères. L’athérosclérose est multifactorielle, mais il est bien établi qu’elle est principalement induite par un excès de cholestérol, en particulier le LDL- cholestérol (aussi appelé « mauvais cholestérol).
La quasi-totalité des méthodes et matériaux de référence permettant d’assurer la traçabilité métrologique et la fiabilité des examens relatifs aux anomalies lipidiques portent sur la mesure du cholestérol total et très peu concernent le LDL-cholestérol (une sous-classe de lipoprotéines). Ces méthodes sont pour la plupart basées sur un couplage chromatographie en phase gazeuse/spectrométrie de masse (GC/MS) avec mise en œuvre de la Dilution Isotopique pour assurer la traçabilité métrologique à la mole. Pourtant, les recommandations de bonnes pratiques relatives à la « Prise en charge thérapeutique du patient dyslipidémique » publiées en mars 2005 par l’AFSSAPS indiquent que « le LDL-C est un meilleur indicateur du risque coronaire que le cholestérol total ». Il n’existe néanmoins à l’heure actuelle qu’une méthode de référence pour le dosage du LDL-C, la Beta-Quantification, validée il y a plus de 10 ans par le « Center for Disease Control » (CDC, Atlanta, USA). Cette méthode peut être considérée comme obsolète en raison de son manque de spécificité et de son caractère indirect, la concentration en LDL-C étant obtenue à partir de celle du cholestérol total et de celle d’une autre sous-classe de lipoprotéines, les HDL (High Density Lipoprotein).
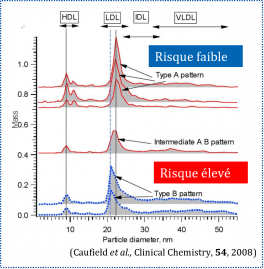
Il s’avère donc nécessaire de développer de nouvelles méthodes primaires de référence pour quantifier les LDL (Low Density Lipoprotein), qui constituent les principaux transporteurs du cholestérol dans le sang. Les LDL sont des assemblages supramoléculaires de forme sphérique dont la taille varie entre 7 nm et 50 nm, qui peuvent être considérés comme des nanoparticules biologiques. Plusieurs études cliniques ont montré que la dangerosité de ces particules dépend de leur taille, les plus petites étant associées à un risque plus élevé de développer des maladies cardiovasculaires.
L’objectif de ce projet a été de développer de nouvelles méthodes de référence et des matériaux de référence certifiés (MRC) pour l’énumération des différentes sous-classes de lipoprotéines. Ces travaux s’inscrivent dans le cadre du projet Européen SIB54 financé dans le cadre de l’EMRP et centré sur l’énumération d’entités biologiques de taille et de natures différentes :
- comptage d’acides nucléiques par PCR (polymerase chain reaction) digitale ;
- énumération de cellules par cytométrie en flux ;
- énumération de particules athérogènes (travaux coordonnés par le LNE).
La principale activité du LNE a consisté à développer une méthode de comptage des lipoprotéines par SMPS (Scanning Mobility Particle Sizer), une méthode habituellement utilisée pour l’analyse de nanoparticules dans le domaine de la surveillance de la qualité de l’air. Une des étapes clés pour le développement d’une telle méthode réside dans la purification des échantillons biologiques.
Le projet a permis de démontrer que le nombre de particules LDL (LDL-P) et le nombre de particules non HDL (non-HDL-P) sont de meilleurs prédicateurs du risque de développer une maladie cardiovasculaire que le LDL-C et une cible complémentaire précieuse pour la thérapie.
En outre, il a été démontré que, pour les lipoprotéines plus petites, le risque de MCV est plus élevé : en plus de la concentration en lipoprotéines, il est donc utile de mesurer la taille des lipoprotéines pour obtenir les données les plus complètes sur le risque de MCV.
Pour répondre au besoin de chaînes de traçabilité dans le domaine des tests avancés de lipoprotéines, des normes appropriées et des méthodes de référence capables de décrire avec précision le profil des lipoprotéines et de fournir de nouvelles informations sur l'évaluation des risques de MCV sont nécessaires. À cette fin, le LNE a mis au point avec succès une plateforme d'analyse de lipoprotéines par ES-DMA (Electrospray-differential mobility analysis) dans le but d'évaluer le potentiel de cette technique à être reconnue comme méthode de référence principale pour le dénombrement absolu des lipoprotéines.
L’organisation d’une inter-comparaison sur les différentes techniques de dénombrement des lipoprotéines a permis de bâtir un réseau de laboratoires experts en analyse de lipoprotéines qui ont émis le souhait que le LNE continue à coordonner les activités relatives à la standardisation des mesures de lipoprotéines à l’échelle mondiale.
Par ailleurs, la méthode de dénombrement de lipoprotéines par SMPS développée au LNE a été validée mi-2016. Néanmoins, la caractérisation de cette méthode développée a montré que celle-ci souffre d’un certain nombre de limitations compromettant sa reconnaissance comme méthode de référence primaire. Malgré cela, cette méthode apporte des informations supplémentaires par rapport aux autres méthodes existantes et pourrait être utilisée avec succès dans un contexte clinique (analyse de cohortes) plutôt que métrologique (établissement de chaines de traçabilité).
Le projet a ensuite consisté à évaluer la comparabilité des dosages par ES-DMA et par d’autres techniques d’analyses avancées de lipoprotéines permettant de déterminer la concentration en nombre de lipoprotéines (RMN, LC/MS/MS, immuno-néphélométrie, etc…). Certaines méthodes ont été appliquées avec succès à l’analyse de cohortes de patients dans le cadre d’essais cliniques (notamment la RMN et l’ES-DMA) mais les résultats obtenus sont parfois discordants. Cette situation est non seulement due au fait que ces différentes méthodes reposent sur des principes physiques différents et ciblent des mesurandes différents.
Aussi, il est apparu nécessaire de comparer les résultats de ces différentes méthodes. Avec le soutien des leaders d’opinion du domaine, les partenaires industriels (Quest Diagnostics, Quantimetrix, Atherotech, LabCorp, LipoScience, Pacific Biometrics) et certains laboratoires académiques (NIH, CDC, Univ Washington, Univ Leiden, CHORI), l’organisation d’une intercomparaison internationale a permis de bâtir un réseau de laboratoires experts en analyse de lipoprotéines. Les résultats ont confirmé que la comparabilité des différentes méthodes de dosage du non-HDL-P était perfectible (CV inter-techniques d’environ 12%).
Ces travaux ont donné lieu à la création d’un nouveau groupe de travail de l’IFCC sur la standardisation des apolipoproteines. Enfin, une collaboration avec l’hôpital de la Pitié Salpetrière et l’Institut Hospitalo-Universitaire cardiométabolique ICAN a eu lieu, pour déterminer si les techniques d’analyse avancée de lipoprotéines permettent de personnaliser le traitement en fonction du profil lipoprotéique des patients et ce d’une manière plus fine que les biomarqueurs conventionnels. Les résultats ont montré que l’analyse avancée de lipoprotéines permet de mieux stratifier les patients.
Impacts scientifiques et industriels
- Proposition d’une nouvelle méthode primaire permettant d’évaluer plus finement le risque de développer des maladies cardio-vasculaires
- Fiabilisation du diagnostic
Publications
Comparability of lipoprotein particle number concentrations across ES-DMA, NMR, LC-MS/MS, immunonephelometry and VAP: In search of a candidate reference measurement procedure for apoB and non-HDL-P standardization. Delatour V, Clouet-Foraison N, Gaie-Levrel F, Marcovina S, Hoofnagle AN, Kuklenyik Z, Caulfield MJ, Otvos JD, Krauss RM, Kulkarni KR, Muniz N, Contois JH, Remaley AT, Vesper HW, Cobbaert CM and Gillery P Clin Chem, 2018;64(10):1485-1495. doi: 10.1373/clinchem.2018.288746
Apolipoprotein B measurement: Need for standardization Contois JH, Delatour V J Clin Lipidol 2018;12(2):264-265 doi.org/10.1016/j.jacl.2018.02.017
Establishing SI-Traceability of Nanoparticle Enumeration Techniques: A Case Study on Electrospray Differential Mobility Analysis Clouet-Foraison N, Gaie-Levrel F, Gillery P, Delatour V.J Anal Bioanal Tech 2017, 8:4 doi: 10.4172/2155-9872.1000370
Advanced lipoprotein testing for cardiovascular diseases risk assessment: a review of the novel approaches in lipoprotein profiling. Clouet-Foraison N, Gaie-Levrel F, Gillery P, Delatour V. Clin Chem Lab Med. 2017;55(10):1453-1464. doi: 10.1515/cclm-2017-0091.
Absolute Quantification of Bionanoparticles by Electrospray Differential Mobility Analysis: An Application to Lipoprotein Particle Concentration Measurements. Clouet-Foraison N, Gaie-Levrel F, Coquelin L, Ebrard G, Gillery P, Delatour V. Anal Chem. 2017;89(4):2242-2249. doi: 10.1021/acs.analchem.6b02909
Communications
Mai 2019 : Congrès IFCC, Barcelone (Espagne): Standardization of advanced lipoprotein testing: the BioSITrace project
Juillet 2018 : Congrès AACC, Chicago (USA) : BioSITrace crossplatform comparison of lipoprotein enumeration methods : towards standardization in advanced lipoprotein testing?
Mai 2019 : Congrès IFCC, Barcelone (Espagne): Standardization of advanced lipoprotein testing: the BioSITrace project
Avril 2017 : Spring Symposium of the Korean Society for Clinical Laboratory; Daejeon, Corée du Sud Laboratory test standardization in clinical chemistry
Aout 2016 Congrès AACC, International Lipoprotein Standardization Forum, Philadelphie (USA). BioSITrace crossplatform comparison of lipoprotein enumeration methods : towards standardization in advanced lipoprotein testing?
Décembre 2015 JCTLM stakeholders meeting, Sevres: Traceable lipoprotein counting for CVD risk assessment
Annual meeting of American Association for Clinical Chemistry, “Development of new reference methods and standards for advanced lipoprotein testing : is measurement traceability achievable?”, V. Delatour, Houston, Etats-Unis, Juillet 2013
Partenaires
LGC (GB), PTB (DE), INRIM (IT), NIB (SL), TÜBITAK (Turq.) LipoScience, Quest Diagnostics, TSI, Maine Standards