Le sixième programme d'action communautaire pour l'environnement, adopté par la décision n° 1600/2002/EC du Parlement Européen, a établi la nécessité de réduire la pollution à des niveaux qui minimisent les effets nocifs sur la santé humaine. Un des leviers pour atteindre les objectifs de qualité de l’air fixés par l’UE consiste à agir sur les émissions liées aux transports (aérien, maritime et routier).
Objectifs
Développer des méthodes de mesure primaires pour l’analyse des PGE émanant du relargage de particules des pots d’échappement catalytiques
Résumé et premiers résultats
Les véhicules automobiles constituent une source majeure de pollution environnementale, à la fois du point de vue des contaminants atmosphériques primaires (CO, NOx, SOx et hydrocarbures), mais également du fait de la libération de nombreux éléments inorganiques lors du processus de combustion. Le mercure (Hg) est naturellement présent dans les combustibles fossiles, alors que les éléments du groupe du platine (PGE) proviennent de l’utilisation des pots catalytiques. Ces métaux (Pt,Pd, Rh) sont en effet utilisés à des teneurs de quelques 1000 mg/kg pour piéger et transformer les polluants primaires ; le rhodium est ainsi majoritairement utilisé pour la réaction de réduction des oxydes d'azote (NOx) alors que les éléments platine et palladium sont actifs pour l'oxydation du monoxyde de carbone (CO) et des hydrocarbures.
Le projet européen ENV 02, financé dans le cadre du programme EMRP, a pour objectif de proposer des développements nécessaires du point de vue de la métrologie afin de mieux comprendre, mieux mesurer et par conséquent mieux contrôler ces émissions de gaz d’échappement automobiles (particules de suie, PGE et Hg0).
La réduction des émissions secondaires de PGE constitue notamment un enjeu important en termes de santé publique, écologique, mais également économique du fait de la rareté de ces éléments et donc de leurs coûts. L’étude de la cinétique d’émission de PGE en ng/km ne pourra par ailleurs être entreprise que si des méthodes primaires de référence sont développées pour la quantification du Pt, Pd et Rh, afin que la traçabilité métrologique des résultats obtenus par des analyses de routine puisse être assurée. Le LNE intervient plus particulièrement sur le développement de ces méthodes de mesure primaires qui mettent en œuvre la spectrométrie de masse ICP et une approche par Dilution Isotopique (DI) ou ajouts dosés, nécessaires pour assurer une traçabilité métrologique directe à la mole, unité du SI pour la quantité de matière.
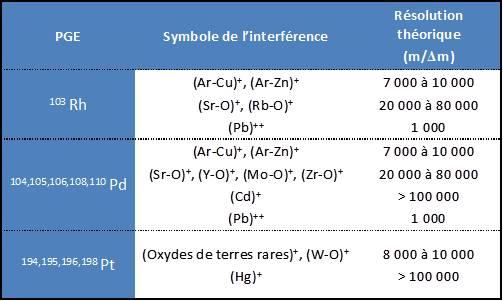
La réalisation d’une étude bibliographique a permis d’identifier les interférences problématiques pour l’analyse par ICP-MS des PGE dans les émissions particulaires automobiles. Compte tenu des résolutions théoriques nécessaires pour le dosage de ces éléments, le développement de méthodes primaires relève d’un véritable défi analytique.
Un protocole préliminaire sur résine échangeuse de cations a été défini afin d’éliminer les interférences isobariques inhérentes à la matrice constituée par ce type d’échantillons. Ce prétraitement se devait d’être compatible avec la mise en œuvre de la méthode primaire de DI pour le Pt et le Pd et celle des ajouts dosés pour le Rh (élément mono-isotopique pour lequel l’approche par DI n’est pas applicable).
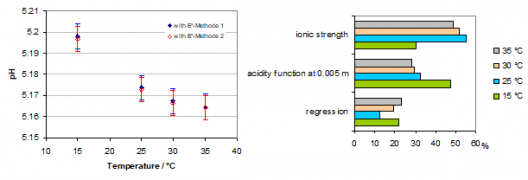
La validation des méthodes a été effectuée principalement sur le matériau de référence (MRC) BCR 723, seul MRC existant avec des teneurs certifiées pour les 3 PGE et dont la matrice est très proche des prélèvements de particules automobiles (poussières de la route prélevées dans un tunnel). Les valeurs obtenues par le LNE sont en très bon accord avec les valeurs certifiées. Les performances requises dans ce projet au niveau des incertitudes (1 % pour le Pt et Pd, et 2 % pour le Rh) semblent cependant, à l’exception du platine, difficiles à respecter pour des teneurs aussi faibles en PGE (quelques ng/g). Les incertitudes relatives obtenues se situent en effet vers 8 à 10 % pour le Rh et Pd et l’homogénéité intrinsèque du matériau de référence BCR 723 n’apparaît pas suffisante pour atteindre les objectifs initiaux. Une procédure d’identification par recherche du Rh, Ir et Os (PGE secondaires) dans les émissions automobiles doit également être établie.
Les procédures développées permettront d’assurer la traçabilité métrologique des résultats de mesure et pourront être utilisées pour la certification des matériaux de référence. Les données ainsi obtenues permettront d’évaluer le taux d’émission de PGE de catalyseurs automobiles dans l’air ambiant.
Site du projet :
Impacts scientifiques et industriels
- Fournir aux équipementiers et constructeurs automobiles des méthodes pour mieux caractériser les émissions de polluants inorganiques et contribuer au développement de pots catalytiques plus respectueux de l’environnement
- Réduire les limites légales fixées pour les polluants atmosphériques provenant des automobiles
- Certifier des matériaux de référence
Publications et communications
LABARRAQUE G., OSTER C., FISICARO P., MEYER C., VOGL J., NOORDMANN J., RIENITZ O., RICCOBONO F. ET DONET S., “Reference measurement procedures for the quantification of platinum group elements (PGEs) from automotive exhaust emissions”, International journal of environmental analytical chemistry, 95, 9, 2015, 777-789, DOI: 10.1080/03067319.2015.1058931.
Partenaires
- PTB (All.),
- BAM (All.),
- JRC (EC)