L’ordonnance du 13 janvier 2010 relative à la biologie médicale rend obligatoire l’accréditation par le COFRAC de tous les laboratoires de biologie médicale (publics comme privés) selon la norme ISO EN 15189 et ce d’ici le 1er novembre 2016. Ce référentiel implique l’utilisation de procédures validées et dont les résultats doivent être raccordés à un étalon national par le biais d’une chaîne de traçabilité métrologique ininterrompue.
Objectifs
Développer et valider des méthodes de référence d’ordre supérieur pour le dosage des principaux biomarqueurs utilisés en biologie clinique
Développer un matériau de référence certifié (MRC)
Résumé et premiers résultats
Il apparaît que contrairement aux autres domaines de la mesure, les résultats des analyses de biologie médicale ne sont à ce jour pas toujours traçables à des références reconnues internationalement (comme par exemple des matériaux de référence certifiés ou des méthodes de référence) et que les incertitudes de mesure ne sont pas systématiquement évaluées.
Cette situation est en contradiction non seulement avec la norme ISO EN 15189, mais également avec d’autres référentiels internationaux, comme notamment la Directive Européenne 98/79/CE qui exige que les produits de diagnostic in vitro soient traçables au Système International d’unités (SI) via des étalons de mesure d'ordre métrologique supérieur. Il est donc nécessaire de disposer de méthodes de référence pour le dosage des principaux biomarqueurs utilisés en biologie médicale.
Le LNE a donc initié depuis 2006 des travaux dans le domaine biomédical afin d’évaluer et d’améliorer la fiabilité des analyses de biologie médicale. Ces travaux ont pour objectif d’assurer la traçabilité métrologique des résultats à des références reconnues internationalement et permettre la comparabilité des résultats dans le temps et d’un laboratoire à l’autre, même s’ils utilisent des techniques différentes. Ils permettent également d’évaluer les performances des méthodes utilisées en routine dans les laboratoires de biologie médicale et d’établir des recommandations concernant les méthodes devant être privilégiées.
Pour cela, la première étape consiste à développer et valider des méthodes de référence d’ordre supérieur pour le dosage des principaux biomarqueurs utilisés en biologie clinique. Compte tenu du nombre considérable de paramètres mesurés en routine en biologie clinique, il a été indispensable de prioriser les biomarqueurs pour lesquels une méthode de référence devait être développée. Ce choix a été effectué en concertation avec les autorités de santé publique (ANSM, HAS, DGS). Les biomarqueurs prioritaires retenus sont ceux associés aux principales pathologies humaines (maladies cardiovasculaires, diabète, …), afin de maximiser l’impact des travaux réalisés.
Ce projet a donc ciblé les activités relatives au dosage des biomarqueurs suivants : glucose, créatinine, hémoglobine glyquée HbA1c, cholestérol total, cholestérol-LDL, cholestérol-HDL et triglycérides, ainsi que le développement d’un matériau de référence certifié (MRC) pour l’ensemble de ces différents paramètres, à l’exception de l’HbA1c. La mise en œuvre de la Dilution Isotopique a permis d’assurer la traçabilité métrologique à la mole, unité du SI pour la quantité de matière.
Impacts scientifiques et industriels
- Evaluation des performances des méthodes utilisées en routine dans les Laboratoires de Biologie Médicale (LBM)
- Amélioration des données de biologie clinique
- Fourniture de valeurs de référence dans le cadre de la réalisation d’essais d’aptitude à destination des LBM (échantillons de contrôle de la qualité de l’ANSM, …)
- Certification d’un matériau de référence
- Evaluation de la justesse des lecteurs de glycémie
- Evaluation de la commutabilité de matériaux d'étalonnage industriels et d’échantillons de contrôle qualité
- Evaluation de la qualité des lots d'étalons fournis par les fabricants
- Transfert des méthodes développées vers les équipes de recherche de CHU
Publications et communications
DELATOUR ET AL, « Development of reference methods for the measurement of biomarkers in France », Ann. Biol. Clin., 68, 6, 2010, 698-699
DELATOUR V., LALÈRE B., DUMONT G., HATTCHOUEL J.-M., FROISSART M., DE GRAEVE J. et VASLIN-REIMANN S., “Development of a reference method for creatinine measurement to improve diagnosis and follow-up of kidney disease”, Revue française de métrologie, 26, 2011, 21-31, DOI: 10.1051/rfm/2011008.
PIERONI L., DELANEY P., BOUTTEN A., BARGNOUX A.-S., ROZET E., DELATOUR V., CARLIER M.-C., HANSER A.-M., CAVALIER E., FROISSART M. et CRISTOL J.-P., “A multicentric evaluation of IDMS-traceable creatinine enzymatic assays”, Clinica Chimica Acta, 412, 23-24, 2011, 2070-2075, DOI: 10.1016/j.cca.2011.07.012.
DELATOUR V., LALÈRE B., SAINT-ALBIN K., PEIGNAUX M., HATTCHOUEL J.-M., DUMONT G., DE GRAEVE J., VASLIN-REIMANN S. et GILLERY P., “Continuous improvement of medical test reliability using reference methods and matrix-corrected target values in proficiency testing schemes: Application to glucose assay”, Clinica Chimica Acta, 413, 23-24, 2012, 1872-1878, DOI: 10.1016/j.cca.2012.07.016.
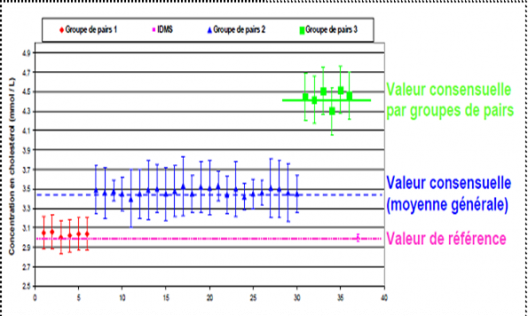
HEUILLET M., LALÈRE B., PEIGNAUX M., DE GRAEVE J., VASLIN-REIMANN S., PAIS DE BARROS J., GAMBERT P., DUVILLARD L et DELATOUR V., “Validation of a reference method for total cholesterol measurement in human serum and assignation of reference values to proficiency testing samples”, Clinical Biochemistry, 46, 4–5, 2012, 359-364, DOI: 10.1016/j.clinbiochem.2012.11.026.
BOUTTEN A., BARGNOUX A.S., CARLIER M.C., DELANAYE P., ROZET E., DELATOUR V., CAVALIER E., HANSER A.M., FROISSART M., CRISTOL J.-P. et PIÉRONI L., “Enzymatic but not compensated Jaffe methods reach the desirable specifications of NKDEP at normal levels of creatinine. Results of the French multicentric evaluation”, Clinica Chimica Acta, 419, 2013, 132-135, DOI: 10.1016/j.cca.2013.01.021
FLAMANT M., VIDAL-PETIOT E., METZGER M., HAYMANN J.P., LETAVERNIER E., DELATOUR V., KARRAS A., THERVET E., BOFFA J.J., HOUILLIER P., STENGEL B., VRTOVSNIK F. et FROISSART M., “Performance of GFR Estimating Equations in African Europeans: Basis for a Lower Race-Ethnicity Factor Than in African Americans”, Am. J. of Kidney Disease, 62, 1, 2013, 182-184, DOI: 10.1053/j.ajkd.2013.03.015.
DELATOUR V., LALÈRE B. et VASLIN-REIMANN S., “Development of reference methods for the measurement of biomarkers”, IMEKO TC Conference (TC8 - TC23 - TC24) “Metrological traceability in the globalisation age”, Paris, France, 6-8 avril 2011.
HEUILLET M., DELATOUR V., LALERE B. et VASLIN-REIMANN S., “How to perform traceable measurements for biomarkers quantification”, 15e Congrès international de métrologie, Paris, France, 3-6 octobre 2011.
DELATOUR V., HEUILLET M., PEIGNAUX M., LALERE B. et VASLIN-REIMANN S., « Apport de la spectrométrie de masse et des méthodes de référence pour le contrôle qualité en biologique clinique », 29es Journées Françaises de Spectrométrie de Masse, Orléans, France, 17–20 septembre 2012.
HEUILLET M., DELATOUR V., PEIGNAUX M., LALERE B., DE GRAEVE J., VASLIN-REIMANN S. et DUVILLARD L., « Développement et validation d’une méthode de référence pour le dosage du cholestérol total et application au contrôle qualité en biologie clinique », 29es Journées Françaises de Spectrométrie de Masse, Orléans, France, 17–20 septembre 2012.
VASLIN-REIMANN S. et DELATOUR V., « Matériaux de Référence Certifiés pour la biologie médicale : une denrée rare en France ? », Journée Technique du Collège Français de Métrologie, Paris, France, 27 novembre 2012.
HEUILLET M., PEIGNAUX M., LALERE B., VASLIN-REIMANN S., DUVILLARD L. et DELATOUR V., “A commutability study coupled to a multicentric analysis of accuracy of total cholesterol, LDL-C, HDL-C and total glycerides assays”, Annual meeting of American Association for Clinical Chemistry, Houston, Etats-Unis, 28 juill.–1er août 2013.
DELATOUR V., HEUILLET M., LALERE B. et VASLIN-REIMANN S., « Production d’un matériau de référence certifié pour le glucose, la créatinine et le cholesterol total et organisation d’une étude de commutabilité couplée à une étude multicentrique de la justesse des dosages de routine », 16e Congrès international de métrologie, Paris, France, 7–10 octobre 2013.
Partenaires
- CHU de Dijon (Cholestérol),
- CHU de Reims (HbA1c, Glucose),
- CHU Montpellier (Créatinine)